汪贻广团队在肿瘤纳米疫苗研究中取得进展
阅读次数: 发布日期:2022-03-31
近日,学术期刊Nano Letters在线发表了北京大学药学院天然药物及仿生药物国家重点实验室汪贻广研究团队的最新研究成果“A pH-/enzyme-responsive nanoparticle selectively targets endosomal Toll-like receptors to potentiate robust cancer vaccination”(pH/酶程序响应型Toll样受体选择性靶向智能肿瘤纳米疫苗)。
在恶性肿瘤的治疗中,以免疫检查点抑制剂、肿瘤疫苗等为代表的免疫治疗已经成为继手术治疗、放射治疗和化学治疗三种传统疗法之后的新兴治疗方法,以其相对高效低毒的特点受到广泛的关注。其中,Toll样受体(Toll-like receptor, TLR)激动剂可作为肿瘤疫苗的优良佐剂,与铝佐剂、乳剂佐剂等临床应用的传统佐剂相比,具有免疫活性高、作用机制明确的优势。但以咪唑并喹啉(IMDQ)为代表的小分子TLR激动剂在全身快速分布,易导致头痛、发热甚至细胞因子风暴等不良反应,目前在临床上只能以乳剂、凝胶剂等外用剂型给药,应用范围受到严重限制。而纳米药物递送系统能够改善小分子药物的药动学行为,实现药物的靶向递送,降低毒副作用。
汪贻广研究团队基于课题组已有的pH超敏感(Ultra-pH-sensitive, UPS)纳米技术平台,设计了一种基于Toll样受体激动的智能肿瘤纳米疫苗(TLR activating nanovaccine, TNV),该纳米疫苗可引流至淋巴结并有效蓄积,被抗原呈递细胞摄取后,依次响应内吞体中的酸性环境及组织蛋白酶,释放出游离IMDQ,从而激活位于内吞体内膜上的TLR7/8,诱导强效的抗肿瘤免疫反应,并降低药物全身分布导致的副作用,实现了免疫佐剂IMDQ的高效低毒递送。
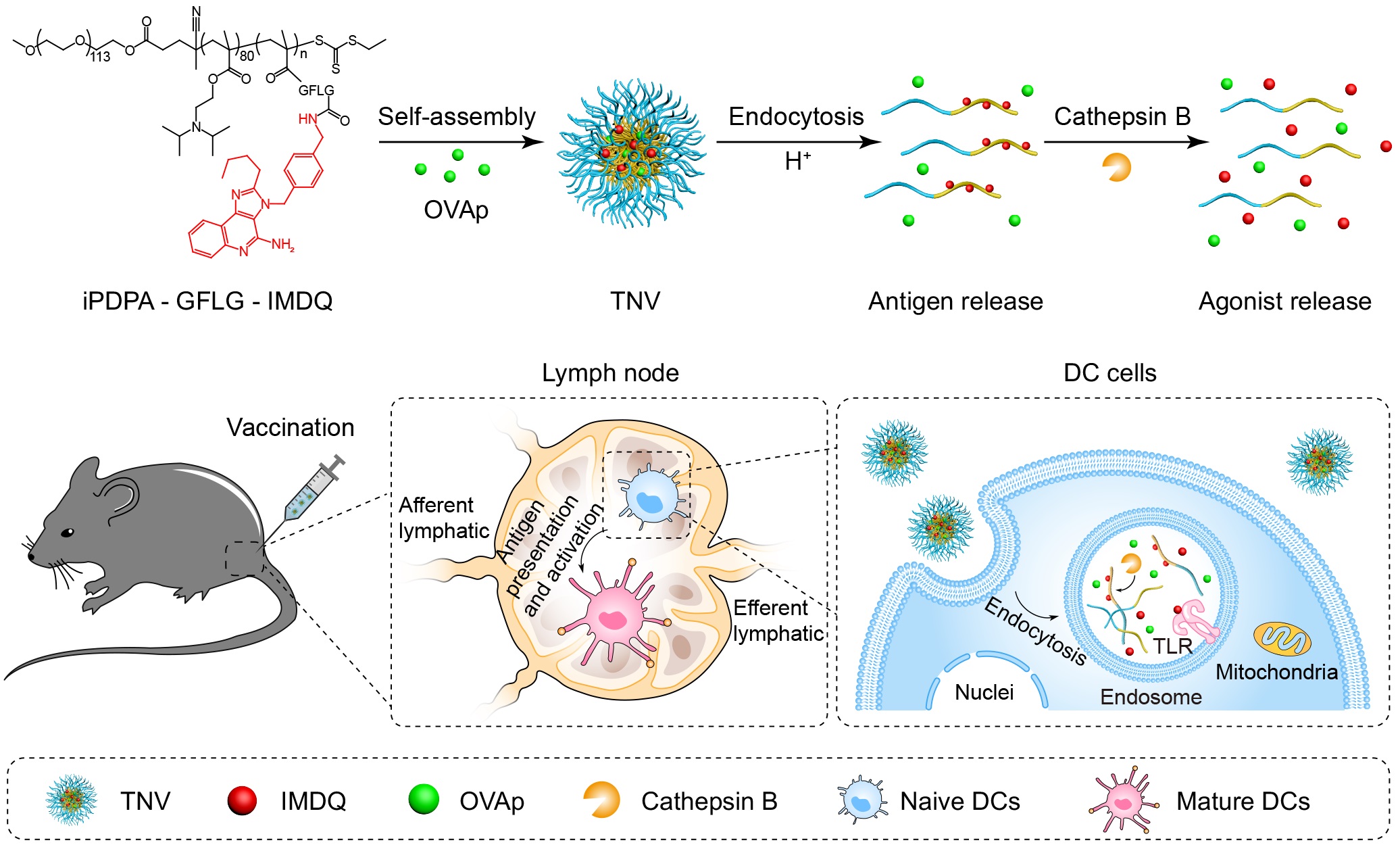
在纳米疫苗TNV中,TLR7/8激动剂IMDQ通过酶敏感键GFLG与UPS聚合物的疏水嵌段共价结合,通过协同性自组装形成纳米胶束。体内实验结果表明,该制剂可蓄积于淋巴结中,对小鼠黑色素瘤和结肠癌均具有良好的肿瘤预防和治疗效应,并且可以诱导小鼠产生特异性免疫记忆,为佐剂的递送和肿瘤疫苗的研发提供了新的设计思路。
北京大学药学院汪贻广研究员为本研究论文的通讯作者。北京大学药学院2021级博士生夏鹤铭和博士后秦蒙蒙为论文的第一作者。论文工作得到国家重点研发计划项目、国家自然科学基金、北京市自然科学基金项目的资助支持。

左起:秦蒙蒙、汪贻广、夏鹤铭
原文链接:https://pubs.acs.org/doi/10.1021/acs.nanolett.2c00185
作者简介:

汪贻广,博士,北京大学研究员、博士生导师,药学院药剂学系主任、天然药物及仿生药物国家重点实验室PI。主要从事智能纳米药物递送及疾病诊疗研究,取得了一系列创新性成果。作为负责人获得国家自然科学基金“优秀青年科学基金”、北京市自然基金“杰出青年科学基金”、国家重点研发计划等资助。先后获得2015年中国药学会-中恒青年药剂学奖、2017年中国药学会-赛诺菲青年生物药物奖。目前担任中国药学会药剂学专委会委员、中国药学会纳米药物专委会委员等。
(北京大学药学院)


