周菁课题组与合作者发现血流扰动致血管内皮损伤的新机制及保护内皮的小分子化合物
阅读次数: 发布日期:2021-11-30
2021年11月30日,北京大学基础医学院周菁课题组在《美国国家科学院院刊》(Proc. Nat. Acad. Sci. USA)在线发表了题为“Vitexin inhibits APEX1 to counteract the flow-induced endothelial inflammation”的研究论文。该研究指出了脱嘌呤/脱嘧啶核酸内切酶-1 (APEX1/Ref-1) 作为流体剪切力响应分子在血流扰动诱导的内皮细胞炎症反应及动脉粥样硬化发生中具有重要作用。课题组利用基因表达谱相似性,筛选到天然黄酮类化合物牡荆素,它能够直接结合APEX1并抑制其活性,从而抑制内皮细胞慢性炎症和动脉粥样硬化的发生。
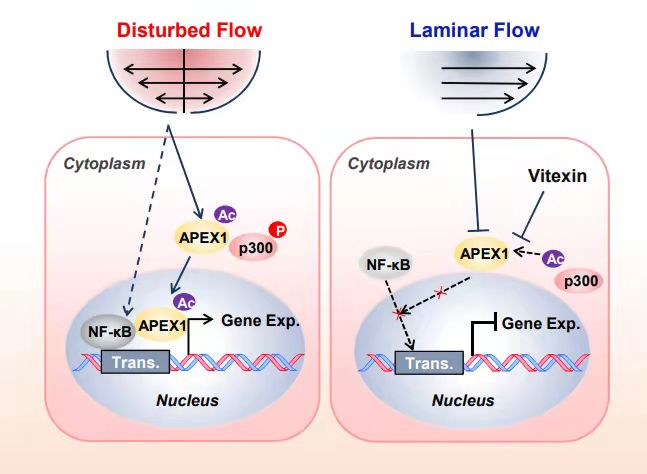
图:牡荆素(Vitexin)通过抑制APEX1入核而抵抗血流扰动诱导的内皮促炎因子表达
血流动力学在动脉粥样硬化发生中发挥关键影响。在动脉分支和弯曲处,血流扰动诱导血管内皮细胞表达促炎分子,吸引循环单核细胞黏附、浸润入动脉壁,平滑肌细胞活化、迁移至内皮下,启动动脉粥样硬化发生。而在大动脉长直部的规则层流对管壁产生抗炎和动脉粥样硬化保护活性。该研究将血管内皮细胞加载模拟层流的脉冲型剪切力(pulsatile shear, PS)和模拟扰流的振荡型剪切力(oscillatory shear,OS)后的表达基因谱与药物基因组学数据库Connectivity Map中已有小分子化合物处理人类细胞后的基因表达谱进行比对,获得了与PS对细胞基因表达影响相似的天然黄酮类化合物牡荆素。利用网络药理学数据库SuperPred预测、细胞热迁移分析、表面等离子共振技术等实验证明了APEX1是牡荆素在内皮细胞中的直接靶分子。
APEX1是DNA碱基切除修复过程中的一种重要核酸修复酶,对维持遗传物质的稳定性和细胞的正常生理活动发挥关键的作用。该研究发现,OS诱导乙酰化酶p300的磷酸化,促进p300与APEX1结合,导致APEX1乙酰化。而乙酰化的APEX1与NF-kB的组分p50和p65形成复合物,转位进入细胞核,促进NF-kB信号通路激活及促炎分子的表达。利用内皮特异性Apex1敲除小鼠合并AAV8-PCSK9病毒注射造高脂血症、ApoE缺陷小鼠,叠加颈动脉部分结扎诱导血流扰动,该研究明确了内皮细胞APEX1的促炎和促动脉粥样硬化发生作用,以及牡荆素的内皮保护活性。该研究揭示了一项血流剪切力调控内皮细胞功能的新机制,并为内皮损伤相关血管病变如动脉粥样硬化的防治研究提供了一种基于力学生物学理论的方案。
周菁课题组长期从事血管稳态和疾病的力学调控机制研究,为本研究奠定了工作基础。北京大学基础医学院周菁研究员与美国加州大学圣地亚哥分校钱煦教授是本研究论文的共同通讯作者。北京大学基础医学院博士后赵川榕博士为本文的第一作者。本研究得到了国家自然科学基金重大研究计划集成项目、创新研究群体项目和面上项目等经费支持。
[延伸阅读]:
原文链接:https://doi.org/10.1073/pnas.2115158118
(基础医学院)


